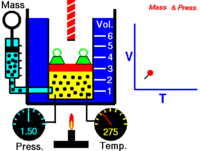
Gesetz von Gay-Lussac
Gase
Basiswissen
Verdoppelt man die Temperatur eines idealen Gases während aber der Druck gleich bleibt, dann wird sich das Gas immer auf das Doppelte seiner vorherigen Volumens ausdehnen. Volumen und Temperatur sind also zueinander proportional. Das ist hier kurz erklärt.
Formeln
- V ~ T
- V/T = konstant
- V₁/V₂ = T₁/T₂
- V₁·T₂ = T₁·V₂
Legende
- T = Temperatur eines idealen Gases, nicht in °C sondern immer in Kelvin ↗
- ~ = Eine Tilde, hier als => Proportionalitätszeichen
- V = Volumen eines idealen Gases, z. B. in Kubikmeter ↗
- T₁ = Temperatur im Zustand 1, z. B. vorher
- T₂ = Temperatur im Zustand 2, z. B. nachher
- V₁ = Volumen im Zustand 1, z. B. vorher
- V₂ = Volumen im Zustand 2, z, B. nachher
- konstant = eine immer feste, also konstante Zahl
Geltungsbereich
Das Gesetz gilt für alle idealen Gase. Ideal nennt man ein Gas, wenn man es so modelliert als gäbe es zwischen den Gasteilchen weder anziehende noch abstoßende Kräfte, als hätten die Gasteilchen kein eigenes Volumen und als würden sie bei Zusammenstößen vollkommen elastisch wechselwirken. Luft bei Raumtemperatur ist fast ein ideales Gas. Benutzt man das Gesetz oben für Luft, enstehen nur sehr klein Fehler. Möchte man diese - kleinen Fehler - vermeiden, modelliert man ein Gas als reales Gas ↗